Es crucial minimizar el riesgo de propagación de los patógenos EHP / tipo-EHP

El Síndrome de Heces Blancas (WFS, por sus siglas en inglés) se refiere a la presencia de filamentos fecales blancos flotantes en los estanques que crían camarones (Penaeus monodon y P. vannamei) en los países del sudeste asiático. Se encuentra que el síndrome está asociado con varios problemas a nivel de granja, que incluyen el retraso en el crecimiento del camarón, las disparidades en el tamaño, la reducción de la alimentación y la mortalidad crónica.
En los países donde se ha reportado WFS, también se han reportado otros patógenos entéricos que también afectan el hepatopáncreas del camarón. Estos incluyen el microsporidio Enterocytozoon hepatopenaei (EHP), la necrosis hepatopancreática aguda que causa Vibrio parahaemolyticus (VpAHPND) y la necrosis hepatopancreática séptica (SHPN) causada por Vibrio sp. La Fig. 1 muestra los países del sudeste asiático donde se han reportado WFS y otras enfermedades entéricas.
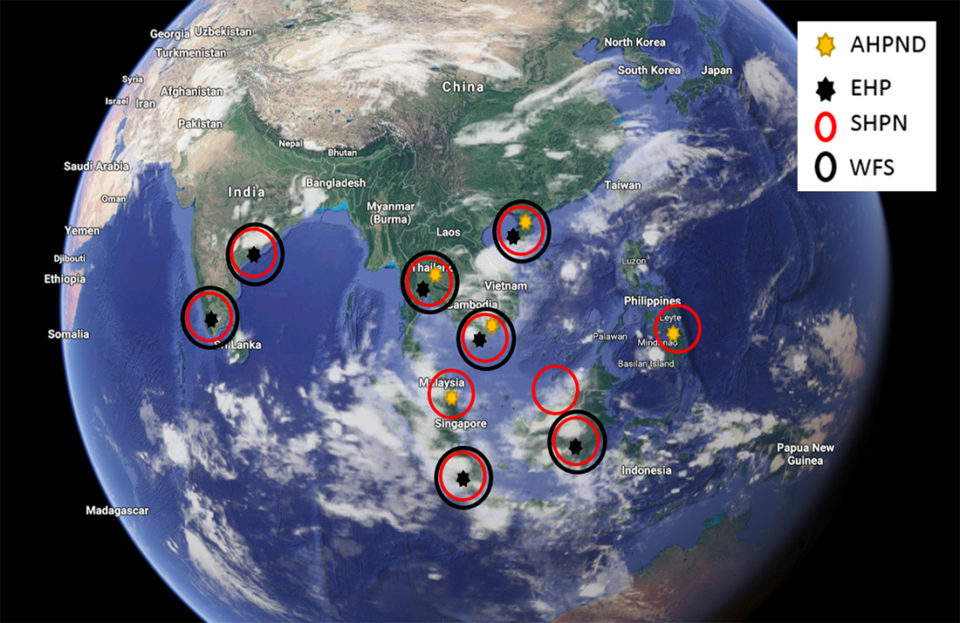
EHP, un microsporidio intracelular que se replica dentro del citoplasma de las células epiteliales del túbulo afectado en el hepatopáncreas, es un patógeno emergente que afecta principalmente al camarón P. vannamei en varios países del sudeste asiático, como Indonesia, Vietnam, China, Tailandia, India y Malasia. Los principales signos clínicos de los camarones infectados con EHP son el retraso del crecimiento, lo que conduce a una mayor variabilidad en el tamaño. En una etapa más avanzada, los camarones infectados con EHP generalmente muestran caparazones suaves, letargo, consumo reducido de alimento y tractos gastrointestinales vacíos. La histología de los tejidos infectados revela varias etapas de desarrollo, incluidas las etapas de plasmodio y esporas.
Varias publicaciones han atribuido la causa de la WFS a diferentes etiologías, como Vibrio cholera, organismos similares a gregarinas, Bacilloplasma sp. y Phascolarctobacterium sp. También se ha propuesto que EHP no es el agente causal de WFS. Sobre la base de estas discrepancias relacionadas con WFS, llevamos a cabo un estudio sistemático para determinar cualquier relación potencial entre WFS y patógenos entéricos, incluido el EHP, en dos regiones diferentes del mundo donde se ha informado sobre EHP.
La primera parte del trabajo se llevó a cabo en un país asiático con un historial de EHP y WFS. Se recogieron muestras de estanques de crecimiento, uno que mostraba WFS y otro donde los camarones no mostraban WFS. Se recogieron muestras de hepatopáncreas y de heces fecales y se analizaron por histología y qPCR para EHP.

El tejido de hepatopáncreas de los camarones de cada estanque de crecimiento se analizó individualmente mediante PCR cuantitativa (qPCR). La Fig. 3 muestra los resultados de las cargas de EHP en animales de estanques que experimentan WFS en lugar de WFS. Cuanto menor sea el valor del umbral de Ciclo (Ct), mayor será la carga de EHP en una muestra.
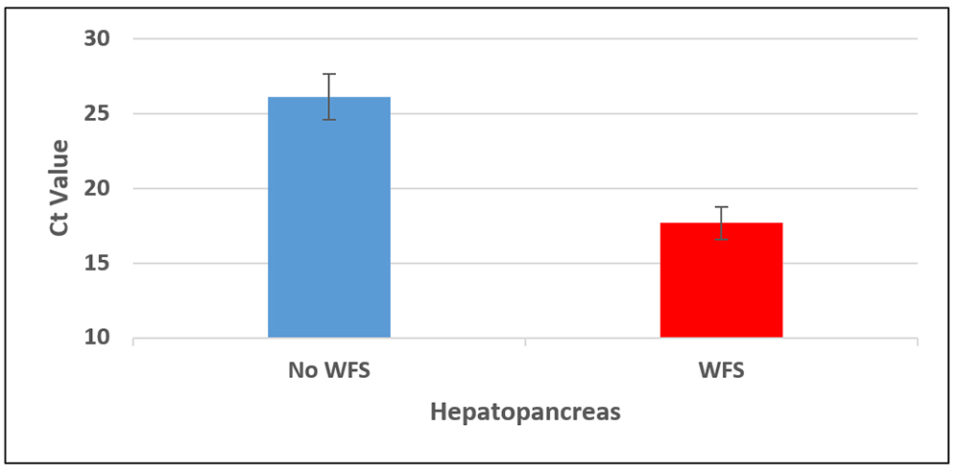
Hay una clara diferencia en el número de copias de EHP entre los dos grupos de animales. El número promedio de copias en el grupo WFS fue de 4×107 copias por ul de ADN frente a 1×105 copias por ul de ADN en estanques sin WFS, lo que representa una diferencia de más de 2 logs. Esto indica que los camarones con WFS podrían ser potencialmente más infecciosos de EHP que los camarones sin WFS. La qPCR en los filamentos fecales del mismo camarón muestra resultados similares; es decir, los camarones que exhiben WFS presentaron un mayor número de copias de EHP en los filamentos fecales que en las cadenas fecales de camarones sin WFS.
Más adelante, en la misma área endémica de EHP, determinamos el número de copias de EHP en muestras de estanques con tres historias diferentes: estanques sin historial de WFS; estanques que muestran WFS; y estanques con una historia de WFS. La Fig. 4 muestra el número de copias de EHP en animales de tres estanques diferentes.
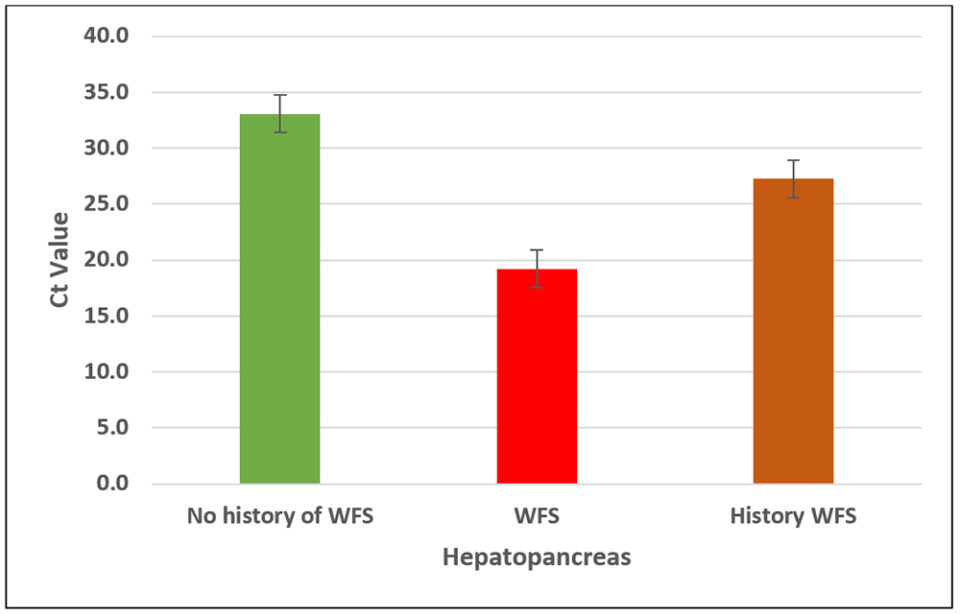
Una vez más, encontramos resultados similares a los obtenidos en el primer experimento. El número de copias de EHP fue mayor en los camarones de los estanques que experimentaron WFS (aproximadamente 1 × 107 copias), seguidos de los estanques con antecedentes de EHP (aproximadamente 4×104 copias) y en los estanques donde no hubo WFS ni se observó ningún signo clínico de enfermedad (alrededor de 4×102 copias).
WFS en las Américas
En el hemisferio occidental, en 2016 informamos la presencia de patógenos EHP y tipo-EHP en camarones de cultivo. El camarón infectado con EHP exhibió signos clínicos similares a los que se muestran en los países del sudeste asiático, incluida la reducción de la alimentación, el crecimiento severamente retrasado y la disparidad de tamaño. Dos años después, describimos el primer caso de WFS en áreas donde previamente informamos la presencia de infección de EHP en Penaeus vannamei cultivado en América Latina. Los filamentos fecales blancos y los camarones que muestran heces blancas a lo largo del tracto gastrointestinal son similares a los encontrados en algunos países del sudeste asiático donde WFS está presente en las regiones endémicas de EHP.
Los camarones que exhiben WFS fueron analizados por H&E y PCR para determinar el agente etiológico asociado a esta patología. Los resultados de PCR y H&E se muestran en la Fig. 5.
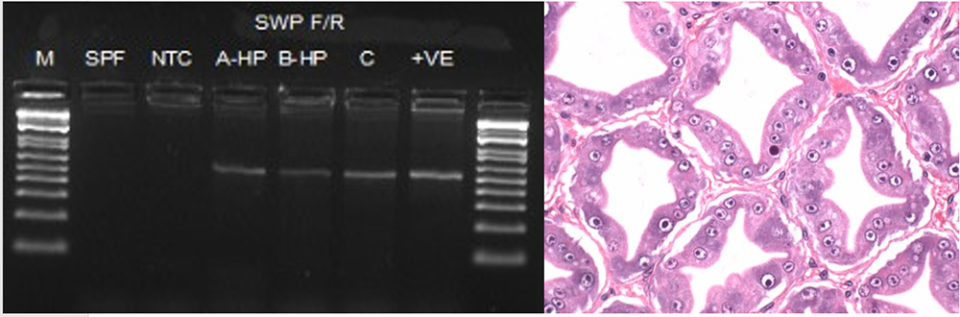
La histopatología del camarón que muestra WFS revela la presencia de estadios de plasmodio y esporas típicos de EHP (Fig. 5b). Las muestras examinadas por PCR anidada para amplificar el gen de la proteína de la pared de la espora (SWP) confirmaron la presencia de EHP.
Papel de SHPN en WFS
Tanto en el sudeste asiático como en América Latina, donde se ha reportado WFS, EHP no es el único patógeno asociado con WFS. Los camarones analizados por H&E muestran, además de EHP, lesiones de Necrosis Hepatopancreática Séptica o SHPN (Fig. 6).
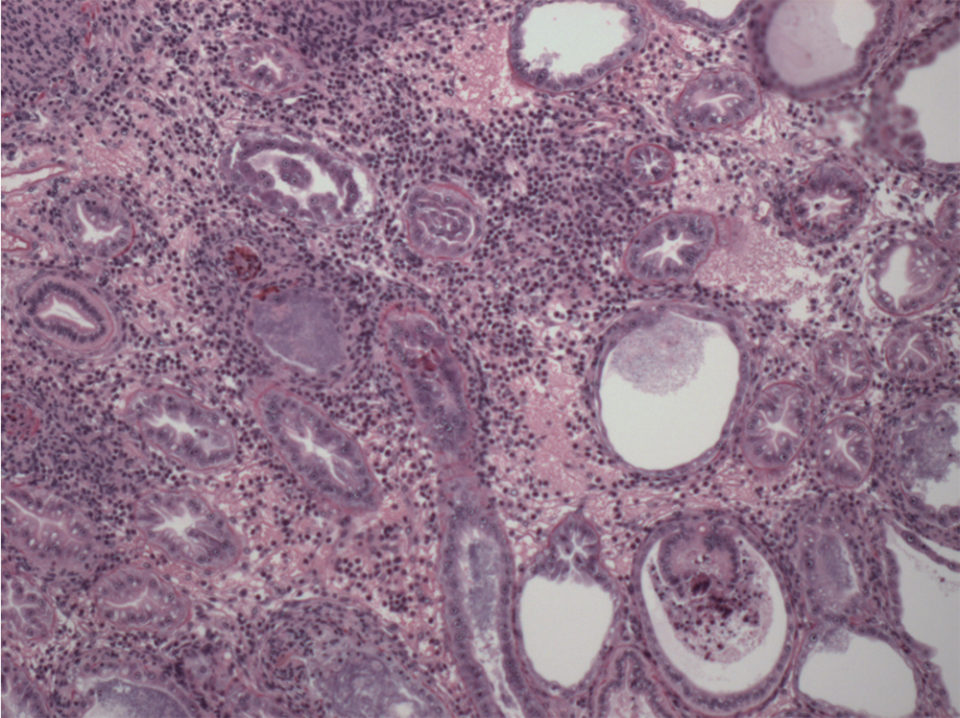
SHPN es una enfermedad bacteriana causada principalmente por Vibrio spp., ya sea patógeno u oportunista. El Vibrio oportunista está siempre en el hepatopáncreas; sin embargo, cuando un patógeno entérico primario causa lesiones en el hepatopáncreas, estos Vibrio spp. oportunistas ganan entrada para colonizar el hepatopáncreas afectado y causar SHPN.
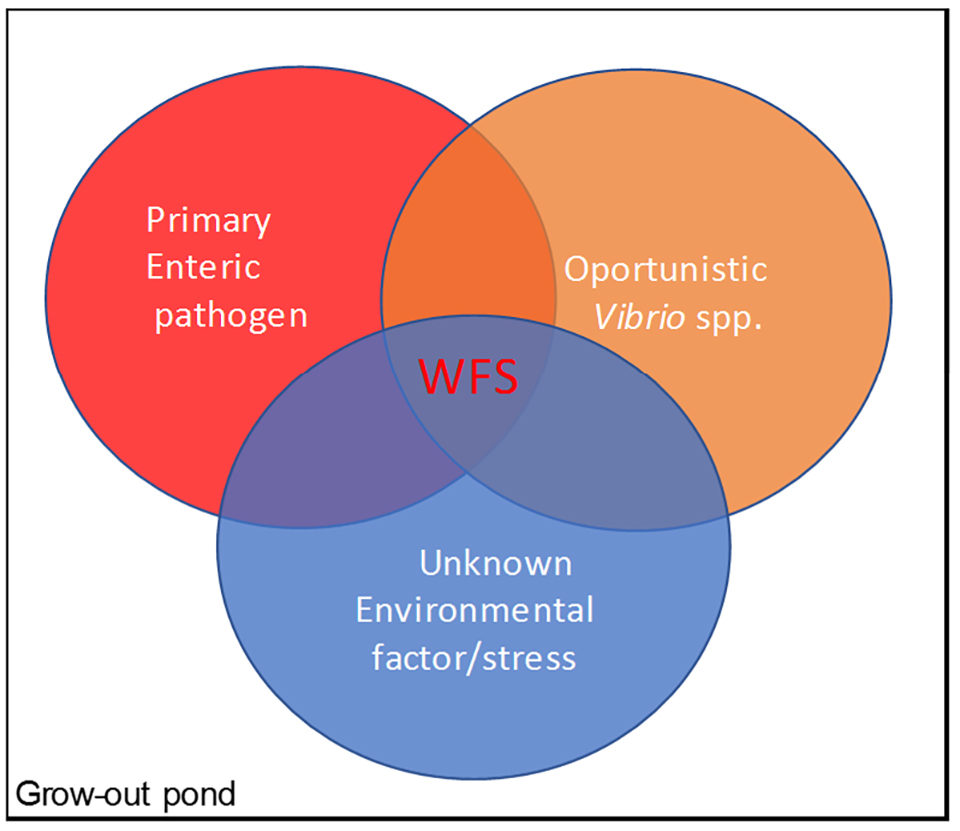
Como muestra la Fig. 7, y en base a nuestro análisis, encontramos una asociación entre WFS, EHP y SHPN en estanques de crecimiento, lo que sugiere que WFS es una posible respuesta fisiológica en camarones afectados por una combinación de patógenos entéricos y posiblemente factores ambientales desconocidos.
El hallazgo de WFS en camarones de cultivo en el hemisferio occidental es importante, ya que podría utilizarse como un predictor de la presencia de EHP. Además, ayudará a dilucidar la fuerte asociación entre un agente similar a EHP / tipo-EHP con la aparición de heces blancas. Como la infección con EHP en etapas tempranas no muestra signos clínicos evidentes, los camarones cultivados en la región deben ser monitoreados de cerca para detectar la presencia de EHP y heces blancas.
Perspectivas
Según nuestro estudio, existe una fuerte asociación entre el síndrome de heces blancas (WFS) y EHP en las regiones endémicas de EHP. El EHP en combinación con otros patógenos entéricos (incluido SHPN) y un posible factor desconocido puede causar el Síndrome de Heces Blancas.
En las áreas endémicas de EHP, los camarones que muestran signos clínicos de Síndrome de Heces Blancas indican un proceso de infección por EHP muy activo en estanques de crecimiento. El Síndrome de Heces Blancas en la industria camaronera en las Américas podría ser un espejo de lo que sucedió en el sudeste asiático hace 15 años, donde EHP ocurrió esporádicamente, pero ahora se ha convertido en uno de los principales factores de riesgo sanitario para la industria camaronera en esta región. Se deben implementar estrategias de bioseguridad para minimizar el riesgo de propagación de patógenos como EHP y tipo-EHP en las Américas.
Ahora que Ud. ha terminado de leer el artículo ...
… esperamos que considere apoyar nuestra misión de documentar la evolución de la industria de acuícola global y compartir nuestra vasta red de conocimiento en expansión de los contribuyentes cada semana.
Al convertirse en miembro de la Global Aquaculture Alliance, se asegura de que todo el trabajo pre-competitivo que realizamos a través de los beneficios, recursos y eventos de los miembros (la Academia, The Advocate, GAA Films, GOAL, MyGAA) pueda continuar. Una membresía individual cuesta solo $ 50 al año.
Authors
-

Luis Fernando Aranguren, Ph.D.
Corresponding author
Aquaculture Pathology Laboratory
School of Animal and Comparative Biomedical Sciences
University of Arizona
1117 E Lowell St.
Tucson, Arizona, 85721, USA
[32,117,100,101,46,97,110,111,122,105,114,97,46,108,105,97,109,101,64,117,103,110,97,114,97,102,108]
-

Hung Mai, Ph.D.
Aquaculture Pathology Laboratory
School of Animal and Comparative Biomedical Sciences
University of Arizona
1117 E Lowell St.
Tucson, Arizona, 85721, USA -

Orlando Pichardo, B.Sc.
Escuela de Ciencias Aplicadas del Mar (ECAM)
Universidad del Oriente (UDP-NE)[32,109,111,99,46,108,105,97,109,116,111,104,64,111,100,114,97,104,99,105,112,114,111,97,108,101,117,122,101,110,101,86]
-

Bambong Hanggono
Fish Health and Environmental Laboratory
Brackishwater Aquaculture Development Center, Situbondo
PO. BOX 5 Panarukan Situbondo Jawa Timur – Indonesia 68351[32,109,111,99,46,111,111,104,97,121,64,111,110,111,103,103,110,97,104,103,110,97,98,109,97,98]
-

Arun K. Dhar, Ph.D.
Associate Professor & Director
Aquaculture Pathology Laboratory
School of Animal and Comparative Biomedical Sciences
University of Arizona
1117 E Lowell St.
Tucson, Arizona, 85721 USA
Tagged With
Related Posts

Health & Welfare
EHP es un factor de riesgo para otras enfermedades del camarón
Desafíos de laboratorio y un estudio caso-control se utilizaron para determinar los efectos de la infección por EHP en dos enfermedades de Vibrio: necrosis hepatopancreática aguda (AHPND) y necrosis hepatopancreática séptica (SHPN).

Aquafeeds
Ingredientes funcionales impulsan la innovación de alimentos para camarones
Los ingredientes y aditivos funcionales promueven el crecimiento, mejoran la salud, y refuerzan la respuesta inmune y otras necesidades fisiológicas de los camarones cultivados.

Health & Welfare
Acuamimetismo: Un concepto revolucionario para el cultivo de camarón
El acuamimetismo simula las condiciones de producción naturales estuarinas mediante la creación de floraciones de zooplancton como nutrición suplementaria para los camarones cultivados, y bacterias beneficiosas para mantener la calidad del agua. Se pueden producir camarones de mejor calidad a un costo menor y de manera más sostenible.

Health & Welfare
Construyendo un mejor pre-criadero de camarones, parte 1
Los sistemas de pre-criadero de camarones ofrecen una oportunidad importante para aumentar los beneficios. Los pre-criaderos adecuadamente diseñados y operados son instalaciones altamente bioseguras para criar postlarvas a densidades muy altas. El objetivo es producir juveniles fuertes, sanos y uniformes con un potencial significativo de crecimiento compensatorio después de su transferencia para el crecimiento final en estanques.

