El compuesto se usa comúnmente para controlar la proliferación de cianobacterias en estanques de peces y camarones

En este artículo, discutiremos las aplicaciones del sulfato de cobre en la acuacultura, las precauciones especiales para su uso, el desarrollo de resistencia al cobre por parte de las cianobacterias, y productos alternativos.
El sulfato de cobre pentahidratado (CuSO4.5H2O), denominado en adelante SC, es la forma de cobre más utilizada para el control de algas en acuacultura debido a su alta solubilidad en agua, disponibilidad y bajo costo. El SC es un sólido cristalino de color azul a temperatura ambiente, que contiene iones de cobre (Cu+2) e iones de sulfato (SO4-2) y cinco moléculas de agua (H2O) en su estructura, de ahí el término “pentahidratado.” El sulfato de cobre es altamente soluble en agua y su solubilidad disminuye a medida que disminuye la temperatura del agua y aumenta el pH del agua. Otra fuente de cobre altamente soluble en agua es el cloruro de cobre dihidratado (CuCl2⋅2H2O), formado por iones de cobre y cloruro (Cl−), y dos moléculas de agua, en forma de cristales verdes. En tiempos de escasez de SC, algunos productores han utilizado óxido de cobre (CuO), disponible en forma de cristales oscuros que van del negro al gris oscuro o al marrón rojizo oscuro; El óxido de cobre es poco soluble en agua y no debe utilizarse.
Aplicaciones del sulfato de cobre en acuacultura
El sulfato de cobre se utiliza principalmente para controlar las cianobacterias (algas verde-azules) en el agua de los estanques. Las densas floraciones de cianobacterias provocan un agotamiento del oxígeno durante la noche y un aumento de las concentraciones de dióxido de carbono, así como una alta fluctuación del pH durante el día. Las cianobacterias también producen sustancias como la geosmina (GSM) y el 2-metilisoborneol (MIB) que pueden impartir un mal sabor a los peces y camarones cultivados. Las cianobacterias también producen microcistinas tóxicas (MC), que son hepatotóxicas (daño hepático provocado por productos químicos) y en altas concentraciones en el agua, causan malestar, perjudican el rendimiento, reducen la inmunidad e incluso pueden causar intoxicaciones agudas y la muerte de peces y camarones. Por lo tanto, es crucial controlar la proliferación de cianobacterias en los estanques de acuacultura.
El sulfato de cobre también es eficaz y económico en el control de infecciones por algunos parásitos, hongos (Saprolegnia sp.) y bacterias externas como Flavobacterium columnare. El SC también se utiliza para controlar algas filamentosas, macrófitos y moluscos acuáticos. Su bajo costo y sus bajas dosis efectivas (entre 0,8 y 2,0 g SC/m2) hacen del SC una de las primeras opciones para el control de algas y el tratamiento de parásitos y otras posibles enfermedades de los peces en grandes estanques.
Consideraciones sobre el uso de sulfato de cobre en estanques piscícolas
Aunque el SC no es un producto peligroso de manipular, se recomienda utilizar guantes, gafas protectoras y ropa de manga larga al manipular el producto y sus soluciones. También es importante almacenar y mantener el producto fuera del alcance de los niños y los animales. Generalmente se pulveriza una solución de sulfato de cobre sobre toda la superficie del estanque o se aplica delante del flujo de agua promovido por aireadores, que favorecen la distribución de la solución química por todo el estanque.
El SC no es muy selectivo para un tipo concreto de algas. Afecta tanto a las cianobacterias como a las algas verdes (clorofitas) de forma indiscriminada. Sin embargo, algunos estudios han demostrado que las concentraciones de SC necesarias para impactar las algas verdes son al menos cinco veces más altas que las de las cianobacterias. Esto es útil, ya que el sulfato de cobre aplicado en las dosis efectivas más bajas para controlar las cianobacterias protegerá a las algas verdes, dándoles la oportunidad de establecerse y superar las poblaciones de cianobacterias en número y biomasa. También mejora la calidad del agua y ayuda a reducir los problemas de “sabores desagradables” en la carne de pescado y camarón.
Factores que afectan la eficiencia de los fertilizantes comerciales en la acuacultura
La toxicidad del cobre (Cu+2) para las microalgas, parásitos y otros organismos acuáticos está regulada por las características químicas del agua, especialmente el pH, la alcalinidad (iones bicarbonato, carbonato e hidroxilo) y la dureza del agua (iones de calcio, Ca+2; e iones magnesio, Mg+2), siendo más tóxico en aguas ácidas y de baja alcalinidad y dureza. Por lo tanto, es importante que el acuacultor comprenda las condiciones químicas del agua del estanque en el momento de la aplicación.
Algunas especies de peces y camarones pueden ser más susceptibles al SC que otras. Por lo tanto, los productores deben conocer la tolerancia de las especies con las que trabajan y realizar bioensayos con un pequeño número de animales de cualquier especie nueva para determinar las dosis efectivas y seguras de SC a utilizar.

Las aplicaciones de SC en tanques y estanques con agua verde pueden provocar déficits de oxígeno disuelto debido a la muerte de microalgas, incluso si la aplicación se realizó para un propósito diferente, como el control de parásitos. Indirectamente, las microalgas se verán afectadas. Por ello, es fundamental controlar los niveles de oxígeno del agua y tener aireadores mecánicos listos para su uso en caso de ser necesario.
La descomposición de las cianobacterias muertas después de los tratamientos con SC aumenta aún más la concentración de geosmina (GEO), 2-metilisoborneol (MIB) y microcistinas (MC) en el agua. Por lo tanto, los tratamientos con SC de los estanques acuícolas conllevan algunos riesgos y pueden aumentar la intensidad del “sabor desagradable,” haciendo que el pescado y el camarón no sean aptos para la venta y el consumo.
Peces como la tilapia del Nilo cultivada en estanques pueden ingerir diariamente grandes cantidades de cianobacterias que contienen GEO, MIB y MC. Por ello, es fundamental realizar un control preventivo y gradual de las cianobacterias y no esperar a que alguna población se establezca fuertemente en un estanque para tomar las medidas adecuadas.
Después de la aplicación de SC, se recomienda no descargar el agua del estanque durante las próximas dos o tres semanas. Esto da tiempo suficiente para que la mayoría de los iones de cobre (Cu+2) formen complejos con carbonatos, hidroxilos y fosfatos presentes en el agua y se asienten en el suelo del fondo del estanque. Una vez depositado en los sedimentos, el cobre queda atrapado en la fracción arcillosa del suelo. Además, al colectar peces con una red de cerco en un estanque (como durante un muestreo o una cosecha), no intercambie ni descargue el agua del estanque para evitar que los efluentes cargados con sólidos (suelo en suspensión, algas y materia orgánica) se liberen a las aguas naturales circundantes. Esta es una práctica eficaz para minimizar la descarga de cobre, otros nutrientes, limo y arcilla y materia orgánica en ríos y otros ambientes acuáticos naturales.
Química del agua y tratamientos de SC
La química del agua influye en la eficacia de los tratamientos con sulfato de cobre. La disociación de los iones de cobre es más rápida en agua de pH bajo (más ácida). En los estanques de acuacultura intensiva, el pH del agua suele ser más bajo (6,0 a 7,5) cerca del atardecer y aumenta a lo largo del día debido a la fotosíntesis de las microalgas, alcanzando a menudo valores superiores a 9,0. Por lo tanto, los tratamientos con SC son más efectivos cuando se aplican temprano en la mañana. La alcalinidad total (TA) es la suma de las bases del agua (principalmente bicarbonato, HCO3–; carbonato, CO3=; e hidroxilo, OH–). Estas bases reaccionan con iones de cobre libres (Cu+2) para formar complejos insolubles, lo que reduce el efecto del cobre sobre las algas y los patógenos específicos. Por esta razón, la dosis de SC debe ser mayor a medida que aumenta la alcalinidad total.
Se sugiere la ecuación SC (g/m3) = TA/100 para estimar la dosis adecuada de SC, asegurando una dosis efectiva con menor riesgo para las especies cultivadas. Por ejemplo, con un TA de 50 mg CaCO3/L, una dosis segura de SC sería 50/100 = 0,5 gramos por metro cúbico. Con una TA de 100 mg CaCO3/L, la dosis segura de SC puede llegar hasta 1,0 gramos por metro cúbico. Sin embargo, cuando la dosis segura estimada a partir de la ecuación es inferior a 0,5 mg por litro, podría no ser suficiente para controlar las microalgas o los patógenos. Por lo general, se necesitan dosis de al menos 0,8 a 1,0 gramos de sulfato de cobre por metro cúbico para un control eficaz de las cianobacterias y los patógenos. Las dosis más pequeñas, incluso con una alcalinidad total más baja, suelen ser ineficaces. Por lo tanto, es fundamental conocer la tolerancia de las especies cultivadas al cobre para establecer una dosis efectiva y segura de aplicación de sulfato de cobre.

En estanques grandes, las dosis de SC aplicadas para controlar parásitos y bacterias externas son las mismas dosis seguras recomendadas para el control de cianobacterias (alrededor de 1 gramo de SC por metro cúbico). En los casos en que la TA supere los 100 mg CaCO3 por litro, se recomienda utilizar la ecuación TA/100 para determinar la dosis. Si TA es 200, la dosis de SC a aplicar debe ser cercana a los 2 gramos por metro cúbico. Para algunos parásitos (por ejemplo, dinoflagelados, protozoos como la ictioftiriasis), así como para el control de hongos y bacterias externas, puede ser necesario realizar de tres a cuatro aplicaciones en intervalos de tres a cinco días. Consulte siempre a un profesional experimentado para definir el protocolo más adecuado para SC y otros productos terapéuticos utilizados en su granja.
El uso adecuado del disco Secchi para evaluar la transparencia del agua es muy importante al calcular las dosis adecuadas de sulfato de cobre.
La densidad de microalgas (cianobacterias) en el agua del estanque también influye en la eficacia del SC. Generalmente se necesitan dosis mayores de SC en aguas excesivamente verdes (con grandes cantidades de algas). Cuando los productores deciden aplicar SC para el control de cianobacterias, el agua del estanque suele tener poca transparencia (de 15 a 25 cm usando un disco Secchi). Con estos valores de transparencia, dosis de SC de entre 0,8 y 1,0 gramos por metro cúbico son suficientes para el control de las microalgas. Sin embargo, con transparencias de agua inferiores a 10 cm, pueden ser necesarias dosis de SC superiores a 1,5 a 2 gramos por metro cúbico.
Tolerancia al cobre y capacidad mutacional de las cianobacterias
Las cianobacterias tienen varios mecanismos para aumentar su tolerancia y sobrevivir con exceso de iones Cu+2 y otros iones metálicos y sustancias tóxicas en el agua. Un mecanismo es la secreción de proteínas (exoproteínas) en una biopelícula que forman en la superficie de sus células. Las exoproteínas atrapan iones metálicos y disminuyen la concentración de iones libres en el ambiente, impidiendo que entren en exceso a las células.
Esto proporciona una protección particular a las cianobacterias frente al cobre, especialmente cuando sus células se agrupan en colonias. Otra es la producción de proteínas específicas que se unen a iones metálicos (metalotioneínas) dentro de las células, reduciendo los efectos tóxicos de los iones Cu+2 que han sido absorbidos. Además, tienen gránulos de polifosfato dentro de sus células, que pueden unirse a iones metálicos como Cu+2, o mecanismos de transporte activo para iones Cu+2 fuera de la célula. Finalmente, un aumento en la producción y actividad de enzimas como la catalasa (CAT) y la superóxido dismutasa (SOD) en respuesta al estrés ambiental provocado por la presencia de iones metálicos como el cobre. Estas enzimas neutralizan las especies reactivas de oxígeno (ROS) dañinas para las células. Las ROS se generan abundantemente en presencia de iones oxidativos como el cobre.
Las cianobacterias frecuentemente expuestas al cobre pueden sufrir cambios genéticos (mutaciones) en los genes responsables de la codificación, producción o expresión de exoproteínas, metalotioneínas y las enzimas CAT y SOD. Los investigadores han informado de mutaciones espontáneas que se produjeron en células de Microcystis aeruginosa después de la exposición a altas dosis de sulfato de cobre. Estos mutantes pudieron prosperar en ambientes con concentraciones de cobre superiores a 0,37 mg Cu+2 por litro, equivalente a 1,5 mg de SC por litro. Otro estudio encontró 1,8 mutantes por cada millón de divisiones celulares. Las cianobacterias en el agua de los estanques pueden superar fácilmente los 2 mil millones de células por litro, y con cada división celular pueden surgir más de 3600 células mutantes por litro. Así, con frecuentes aplicaciones de cobre en estanques y la eliminación constante de las células originales, en unas pocas generaciones podría establecerse una población de cianobacterias predominantemente resistentes al cobre.
En un estudio bajo condiciones controladas de laboratorio, se demostró que en unos pocos ciclos de cultivo la tolerancia de la cianobacteria Microcystis aeruginosa al cobre aumentó de 4 a 12 veces, alcanzando niveles de tolerancia cercanos a 0,8 mg Cu+2 por litro (equivalente a 3,2 mg SC por litro). Una población específica de Microcystis toleró hasta 1,9 mg Cu+2 por litro (equivalente a 7,5 mg SC por litro). Y en una prueba práctica con agua rica en Microcystis aeruginosa recolectada de un estanque de piscicultura comercial, la dosis comúnmente aplicada de 1 mg de SC por litro no redujo el recuento de cianobacterias en comparación con el control. Esto sugiere que la población de Microcystis en esa granja ha desarrollado resistencia al sulfato de cobre debido a su uso repetido. En el mismo ensayo, los tratamientos con peróxido de hidrógeno a 15 y 30 ppm fueron muy efectivos en el control de cianobacterias (Fig. 1). Varios otros estudios indican que el peróxido de hidrógeno en dosis entre 5 y 15 ppm controla selectivamente las cianobacterias en estanques de piscicultura.

Dosis letales y seguras de cobre para tilapia y camarón marino
Para la tilapia del Nilo (Oreochromis niloticus), se determinó para alevines (peso 10 mg, longitud 7 mm) la concentración letal de iones cobre (Cu+2) que mata a la mitad de los animales en 96 horas (CL50-96h) a 0,05 mg Cu+2 por litro usando cloruro de cobre (0,125 mg CuCl2 por litro) y 0,12 mg Cu+2 por litro usando nitrato de cobre (0,457 mg por litro Cu(NO3)2). Para juveniles de 3 gramos, en agua con pH 8,2 y alcalinidad total de 196 ppm, la CL50-96h se estimó en 7,94 mg Cu+2 por litro con sulfato de cobre (31,2 mg por litro CuSO4.5H2O). Para juveniles de tilapia de 90 días de edad, en agua con pH 7,25 y dureza total de 255 ppm, la CL50-96h se estimó en 35 mg Cu+2 por litro con sulfato de cobre (100 mg por litro CuSO4.5H2O). Generalmente se considera segura una concentración equivalente al 5 por ciento de CL50-96h.
Para el camarón blanco del Pacífico (Litopenaeus vannamei), se evaluó la tolerancia al cobre en diferentes etapas de vida en agua con 15 ppt de salinidad y pH de 7,5 a 8,0. La tolerancia al cobre aumentó con las etapas de desarrollo. Para los nauplios, la fase más sensible, la CL50-24h osciló entre 9,5 y 15 microgramos de Cu+2 por litro (o partes por mil millones). En los estadios de zoea, la CL50-24h varió entre 16 y 32 µg Cu+2 por litro. Para las etapas 1, 2 y 3 de mysis, la CL50-48h promedio fue de 85, 200 y 370 microgramos de Cu+2 por litro, respectivamente. Para PL5 (postlarvas de cinco días), la CL50-96h osciló entre 0,64 y 1,5 mg Cu+2 por litro, y entre 1,1 y 2,3 mg Cu+2 por litro para PL10-15. Para camarones de 9 gramos, la CL50-96h osciló entre 4 y 3,1 mg Cu+2 por litro. En un estudio con agua de mar pura, la CL50-96h para 2 g de camarón fue de 35 mg Cu+2 por litro.
La supervivencia de los camarones se evaluó bajo exposición continua a concentraciones de cobre de 10, 5, 2,5 y 1 por ciento de la CL50-96h de 35 mg Cu+2 por litro. La mortalidad total ocurrió dentro de las 6 semanas en camarones expuestos continuamente a concentraciones iguales o superiores al 2,5 por ciento de CL50-96h, es decir, 0,88 mg Cu+2 por litro (equivalente a 3,6 mg SC por litro). Los camarones expuestos continuamente al 1 por ciento de CL50-96h (0,35 mg Cu+2 por litro o 1,4 mg SC por litro) tuvieron una supervivencia del 100 por ciento. Estos dos estudios tuvieron resultados contrastantes con respecto a la tolerancia al SC de los juveniles de L. vannamei, que parece ser mucho mayor con mayor salinidad del agua. Las aguas naturales con mayor salinidad (como el agua de mar) generalmente tienen mayor alcalinidad y dureza total que las aguas de baja salinidad. Los problemas de cianobacterias en las granjas camaroneras ocurren en aguas de baja salinidad, donde los valores de dureza y alcalinidad son mucho más bajos. Así, dosis efectivas de SC de 0,8 a 1,2 gramos por metro cúbico, equivalentes a 0,2 a 0,3 mg Cu+2 por litro, alcanzan inicialmente concentraciones de cobre entre el 10 y el 30 por ciento de la CL50-96h determinada para L. vannamei a 15 ppt de salinidad (1,1 y 3,1 mg por litro de Cu+2 por litro).
Por lo tanto, para el cultivo de L. vannamei en aguas de baja salinidad es importante comprobar la alcalinidad y dureza del agua del estanque que se va a tratar con SC. De hecho, antes de aplicar el producto en todo un estanque, es aconsejable realizar una prueba preliminar de la dosis objetivo de SC con algunos animales en un recipiente pequeño (tanque de 1 metro cúbico, por ejemplo) con la misma agua del estanque a ser tratado.
Los esfuerzos para abordar los sabores desagradables en peces de RAS están fuera de serie
Alguicidas y parasiticidas alternativos al sulfato de cobre
El SC se puede utilizar en dosis bajas y es económico y fácil de conseguir. Es eficaz para el control de algas, algunos parásitos y otros patógenos potenciales. Sin embargo, su uso recurrente en granjas acuícolas favorece el establecimiento de cianobacterias resistentes al Cu+2 y, posiblemente, de parásitos y patógenos más tolerantes. Esto ya está sucediendo en muchas granjas, lo que requiere la aplicación de dosis más altas de SC. Las dosis efectivas de SC utilizadas para controlar las cianobacterias y los patógenos ya están muy cerca de las concentraciones tóxicas de cobre para algunas especies de peces y camarones. Un aumento adicional de las dosis aumentará el riesgo de utilizar SC. Además, se deben esperar mayores niveles de cobre en los sedimentos y efluentes de los estanques con el uso continuo de SC. Esto plantea preocupaciones ambientales con respecto a los posibles efectos nocivos del cobre en organismos acuáticos no objetivo en aguas naturales que reciben efluentes de acuacultura. En consecuencia, es necesario encontrar alternativas al SC para el control de cianobacterias y patógenos de peces en grandes estanques.
El Diurón (diclofenil-dimetil-urea) es un herbicida que tiene acción selectiva contra las cianobacterias preservando otras microalgas. El Diuron fue registrado en EE. UU. para controlar la proliferación de algas en estanques de peces y tiene un costo muy atractivo, lo que lo hace aún más económico por aplicación que el SC. Su dosis efectiva ronda los 0,01 mg de principio activo (AI) por litro. En la práctica, 0,01 gramos de AI por metro cuadrado o 100 gramos de AI por hectárea, para un producto cuestan cerca de (reales brasileños) R$ 7,00 (US$ 1,42)/ha por aplicación, frente a R$ 350,00 (US$71)/ha para SC a 1 gramo de SC por metro cuadrado o 10 kg de SC por hectárea.
Sin embargo, al igual que el SC, el Diurón también tiene una alta persistencia ambiental y su uso continuo puede afectar a organismos no objetivo. También existen preocupaciones sobre su acumulación en la carne de pescado después de repetidas aplicaciones en estanques, y sus residuos también pueden afectar a las comunidades acuáticas en cuerpos de agua que reciben efluentes de granjas acuícolas. Al igual que el SC, el uso repetido de Diuron puede provocar el desarrollo de poblaciones de cianobacterias resistentes a este herbicida, como se ha demostrado en varios estudios, haciendo que el producto sea menos eficaz con el tiempo. Aunque está aprobado por la Agencia de Protección Ambiental de EE. UU. (EPA), hay indicios de que el Diuron tiene efectos cancerígenos y otros riesgos para la salud humana, y los problemas ambientales y de salud humana seguirán ejerciendo presión sobre el uso de Diuron y otros productos químicos. en acuacultura.
El Peróxido de Hidrógeno (HP, H2O2) puede reemplazar al sulfato de cobre. HP es muy eficaz para reducir las cianobacterias en estanques de acuacultura. Las formulaciones líquidas concentradas con 30 o 50 por ciento de HP y Percarbonato de Sodio (conocido como “oxígeno en polvo”) están aprobadas en EE. UU. y países europeos para aplicaciones en acuacultura. El HP también está aprobado para reducir las cianobacterias y compuestos olorosos en el agua que ingresa a las plantas de tratamiento para consumo humano, así como para reducir los olores (provocados por sulfuro de hidrógeno, metano y otros compuestos volátiles), cianobacterias y microorganismos patógenos en los efluentes de las plantas de tratamiento de aguas residuales. El HP reacciona rápidamente con células de microalgas y material orgánico suspendido, descomponiéndose en oxígeno y agua sin dejar residuos tóxicos en el medio ambiente. Una ventaja sobre el SC y otros productos para controlar las cianobacterias es que el HP oxida simultáneamente microcistinas, geosmina (GEO), 2-metilisoborneol (MIB) y probablemente otros compuestos tóxicos y olorosos en el agua.
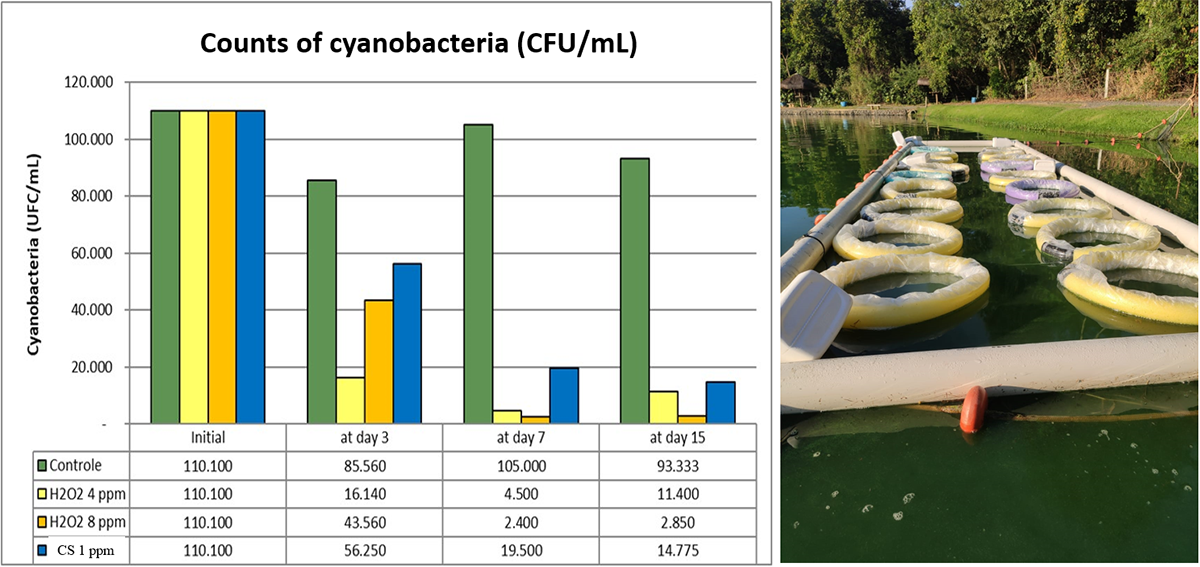
Por lo tanto, el HP ayuda a reducir la intensidad del “mal sabor” y el riesgo de intoxicación por pescado. El HP ya se usa ampliamente para tratar hongos (Saprolegnia sp.) e infecciones bacterianas en huevos de peces (trucha, salmón, bagre y tilapia) y también es eficaz en el tratamiento de parásitos (protozoos, dinoflagelados y monogeneos), hongos y enfermedades externas. bacterias en estanques grandes, así como en baños cortos concentrados. En consecuencia, el peróxido de hidrógeno es una alternativa al SC para la mayoría de sus aplicaciones en acuacultura, con la ventaja de no dejar residuos en los peces ni en el medio ambiente. Dosis de HP de 4 a 15 ppm (4 a 15 g de H2O2 por metro cúbico) son efectivas para controlar las cianobacterias en estanques de peces y son muy seguras para la mayoría de las especies de peces de aguas cálidas. Hemos observado resultados efectivos con el uso de HP en dosis de 4 a 8 ppm (Fig. 2). Una dosis de peróxido de hidrógeno de 4 ppm tiene un costo de producto por aplicación similar al de 1 ppm de SC.
Consideraciones finales
Aunque el SC es eficaz y económico para controlar algas y parásitos, su uso repetido y la necesidad de dosis mayores pueden presentar riesgos para los ecosistemas acuáticos. Al no tener una acción selectiva, acaba afectando a otros organismos benéficos. Y la acumulación de cobre en los sedimentos y su potencial para contaminar cuerpos de agua genera preocupación sobre el impacto ambiental del uso de sulfato de cobre.
Dada la creciente demanda por la adopción de prácticas de producción más sustentables, reduciendo los impactos ambientales y mejorando la seguridad alimentaria, el sector acuícola debe ser sensible y abierto a la necesidad de productos o prácticas de manejo alternativas que puedan reemplazar el uso de químicos como el sulfato de cobre debido a sus posibles impactos.
Ahora que Ud. ha llegado al final del artículo...
… por favor considere apoyar la misión de la GSA de promover prácticas responsables de productos del mar a través de la educación, la defensa y las garantías de terceros. El Advocate tiene como objetivo documentar la evolución de las prácticas responsables de productos del mar y compartir el amplio conocimiento de nuestra amplia red de colaboradores.
Al hacerse miembro de la Global Seafood Alliance, está asegurando de que todo el trabajo pre-competitivo que hacemos a través de los beneficios, recursos y eventos para miembros pueden continuar. La membresía individual cuesta solo $50 al año.
¿No es miembro de la GSA? Únase a nosotros.
Author
-

Fernando Kubitza, Ph.D.
Jundiaí, São Paulo, Brasil
El Dr. Fernando Kubitza es un especialista en acuicultura brasileño y director de Acqua Imagem, www.acquaimagem.com.br, empresa líder desde hace 25 años en proyectos, capacitación y soporte técnico de acuacultura en Brasil.[32,114,98,46,109,111,99,46,109,101,103,97,109,105,97,117,113,99,97,64,111,100,110,97,110,114,101,102]
Tagged With
Related Posts

Intelligence
Consideraciones para el cultivo de tilapia en ambientes de agua salada
Las tilapias se cultivan en una variedad de sistemas de producción, pero principalmente en aguas dulce y de baja salinidad. Pero las tilapias son un excelente candidato para la acuacultura en aguas salobres y marinas porque pueden tolerar una amplia gama de salinidad del agua.

Health & Welfare
El fitoplancton es un componente crítico de los ecosistemas de estanques acuícolas
Los organismos fitoplanctónicos, o microalgas, son muy abundantes en los estanques de acuacultura y tienen un papel crítico en estos ecosistemas, influyendo significativamente en la ecología general del estanque y en la calidad del agua. El manejo adecuado de las poblaciones de fitoplancton es esencial para el éxito de la producción de estanques acuícolas.

Responsibility
La preparación del estanque de camarones es crucial para la producción y prevención de enfermedades
La prevención de enfermedades es una preocupación importante en el cultivo de camarón. La preparación de estanques se enfoca en evitar el arrastre de organismos de enfermedades de un ciclo de cultivo al próximo.

Responsibility
Dinámica del oxígeno disuelto
El manejo del oxígeno disuelto es el requisito más importante de la calidad del agua de los estanques acuícolas. La concentración de OD por debajo de 3 mg/L es estresante para el camarón.


![Ad for [BSP]](https://www.globalseafood.org/wp-content/uploads/2025/07/BSP_B2B_2025_1050x125.jpg)